Использование и хранение гашеной извести
Для снижения образовавшейся плотности погашенной извести, в нее еще добавляют воды. Всю массу тщательно перемешивают, и все повторяется до тех пор, пока содержимое не будет впитывать жидкость. Вода, добавленная в последний раз, должна полностью исчезнуть из поверхности. В конце получившийся состав нужно засыпать песком мелкой фракции, слой которого 20 см не меньше.
Если говорить о хранении гашеной извести в зимнее время, то во избежание замерзания теста в этот период, сверху на песок помещают не меньше 7 см простой земли. Такая яма, в которой находится гашеная известь, должна быть обязательно как-то помечена. Чаще всего ее чем-то ограждают и выдерживают до тех пор, пока даже самые мелкие частицы окончательно не вступят в реакцию с водой. Почему? Если использовать известь, в которой будут непогашенные крупицы, то в растворе могут образоваться нежелательные каверны и вздутия.
Обратите внимание! Когда материал должен предназначаться для кладочного раствора, то хранить его в яме при всех условиях нужно не меньше, чем две недели. А если тесто нужно использовать для приготовления раствора, которым будут штукатурить стены, то срок увеличивается в два раза, и составляет минимум 1 месяц
Количество теста, которое можно получить после процесса гашения, полностью зависит от качества первоначальной негашеной извести (CaО). Из 1 кг кипелки первого сорта может получиться 2 и более литра густого теста. Соответственно, если качество исходного сырья ниже, то результат на выходе будет меньшим. Например, из 1 кг второго и третьего сорта может получиться до 2 и 1,5 л.
Чтобы вы поняли разницу, то обычный строительный раствор представляет собой смесь вяжущего вещества, наполнителя и воды. А вот известняковый раствор имеет в своем составе тесто, песок и воду. Его довольно часто используют в строительстве, так как известняковый раствор славится повышенной адгезией с кирпичными и шлакобетонными поверхностями. Кроме того, такую смесь используют даже на деревянных стенах. Только их предварительно нужно подготовить, набив дранку или сетку для штукатурки.
Индивидуальные доказательства
- ↑ запись на в базе данных вещества GESTIS из в IFA , доступ к 14 февраля 2017 года. (Требуется JavaScript)
- Технический паспорт (PDF) от Merck , по состоянию на 19 января 2011 г.
- Дэвид Р. Лид (Ред.): Справочник по химии и физике CRC . 90-е издание. (Интернет-версия: 2010 г.), CRC Press / Taylor and Francis, Boca Raton, FL, Index of Refraction of Inorganic Crystals, pp. 10-245.
- Вальтер Эренрайх Трегер: Оптическое определение породообразующих минералов . 2-е издание. Лента2 . Швейцарская борода, Штутгарт 1969, стр.69 .
- Юрген Мартин: «Ульмер Вундарзней». Введение — Текст — Словарь по памятнику немецкой специальной прозы XV века. Königshausen & Neumann, Würzburg 1991 (= Медико-историческое исследование Вюрцбурга. Том 52), ISBN 3-88479-801-4 (также медицинская диссертация Вюрцбург 1990 г.), стр. 141.
- Вильгельм Hassenstein, Герман Virl : фейерверочная книга от 1420 600 лет немецкого порохового оружия и оружейным. Перепечатка первой гравюры 1529 г. с переводом на верхненемецкий язык и пояснениями Вильгельма Хассенштейна. Verlag der Deutsche Technik, Мюнхен, 1941, с. 109.
Получение
Оксид кальция также называют жжёной известью из-за способа получения. Получают негашёную известь путём нагревания и разложения известняка – карбоната кальция (CaCO3).
Реакция получения оксида кальция из известняка выглядит следующим образом:
CaCO3 → CaO + CO2.
Кроме того, негашёную известь можно получить двумя способами:
- из простых веществ, наращивая оксидный слой на металле –
2Ca + O2 → 2CaO; - при термической обработке гидроксида или солей кальция –
Ca(OH)2 → CaO + H2O; 2Ca(NO3)2 → 2CaO + 4NO2 + O2.
Реакции протекают при высоких температурах. Температура сожжения известняка – 900-1200°C. При 200-300°C на поверхности металла начинает образовываться оксид. Для разложения солей и гидроксида необходима температура в 500-600°C.
Применение и использование мела:
Мел используется в быту и различных отраслях народного хозяйства:
- в строительстве и для ремонта зданий и сооружений – для побелки, окраски заборов, стен, бордюров и пр.,
- для защиты стволов деревьев,
- в сельском хозяйстве для известкования кислых почв,
- как необходимый компонент мелованной бумаги, используемой в полиграфии для печати качественных иллюстрированных изданий,
- для письма на больших (школьных и пр.) досках для общего обозрения,
- в фармацевтике в лекарственных препаратах как вспомогательное вещество (наполнитель),
- в животноводстве как кормовая добавка, обеспечивающая необходимое количество кальция в рационе птиц и скота,
- в качестве дисперсного наполнителя для полимерных композиций (полипропилена, полиэтилена и пр.), резины, керамики и пр.,
- при производстве строительных материалов – извести, портландцемента, стекла и пр.,
- в пищевой промышленности – для очистки свекловичного сока,
- в парфюмерии и косметике – в качестве наполнителя,
- и пр.
Ссылка на источник
Главные составляющие компоненты
В состав минеральной породы входит большое количество компонентов. К ним относят:
- Участки скелетов — около десяти процентов. Это не только частицы простейшей группы растений, но также остатки от многоклеточных организмов.
- Раковины древних моллюсков — содержится около десяти процентов. Сюда также включают животных с панцирем, состоящим преимущественно из известняка — фораминиферы. Фораминиферы — одноклеточные, раковины которых и стали главной частью формирования современных залежей минерала. После смерти таких организмов их панцири шли ко дну океана, а после создавали фораминиферовые известняки. Спрессованные под действием течений и воды, остатки раковин моллюсков на протяжении больного количества лет дополнялись остатками животных организмов, а также рыбами. Несмотря на то, что ещё в 1953 году учёные выявили, что главная роль в формировании известняковых минералов отводится растительным культурам, до сих пор существует мнение, что главными в таком процессе всё-таки считаются фораминиферы.
- Частички нароста водорослей — всего около сорока процентов. Большая часть пород, по мнению многих, возникла из остатков простейших культур — кокколитофоридов, а не из раковин моллюсков. Кокколитофориды до сих пор существуют и комфортно обитают на просторах мирового океана, активно участвуя в процессе обмена углерода между водами океана и самой атмосферой.
- Мелкие кристаллы калия не превышают пятидесяти процентов. Эти минералы природного происхождения возникли в результате сложных процессов образования.
- Силикаты нерастворимого характера включены в состав породы в количестве трёх процентов. Это минералы преимущественно геологического происхождения — песок, остатки от горных пород, которые переносятся в отложениях мела посредством ветра либо воды.
Разновидности
Строительная известь делится на два типа: воздушный и гидравлический. Воздушная известь делает возможным застывание бетона в обычных условиях, а гидравлическая – и в сухих условиях, и в водной среде. Поэтому воздушная известь пригодна для проведения наземных работ, а гидравлическая – для возведения опор мостов.
Исходя из нюансов обработки обожженного материала, выделяют известь различных видов:
- Комовая известь изготавливается в виде смеси разных по размеру кусков. Она состоит главным образом из оксидов кальция (преобладающая часть) и магния. Также в ее состав могут входить алюминаты, силикаты и ферриты магния или кальция, которые формируются при обжигании, и карбонат кальция. Функцию вяжущего ингредиента она не выполняет.
- Молотую известь делают, перемалывая комовую известь, поэтому их состав практически идентичен. Она используется в негашеном виде. Это позволяет избежать появления отходов и ускорить затвердение. Изделия из нее имеют прекрасные прочностные свойства, они водостойки и отличаются высокой плотностью. Чтобы ускорить процесс затвердения материала, добавляют хлористый кальций, а чтобы замедлить застывание – серную кислоту или гипс. Это позволяет предупредить появление трещин после высыхания. Транспортируется молотая известь в герметичных емкостях из бумаги или металла. Хранить ее разрешается не больше 10-15 дней в сухих условиях.
- Гидратная известь – высокодисперсное сухое соединение, формирующееся при гашении извести. В ее состав входят гидроксиды кальция и магния, карбонат кальция и иные примеси.
- При добавлении жидкости в объеме, которого хватает, чтобы оксиды превратились в гидраты, образуется пластичная масса, имеющая название известкового теста.
Самыми популярными в использовании на сегодняшний день являются гашеная и негашеная извести.
Фото различных видов негашеной извести
Химическая формула и состав извести
Для производства извести не применяется никаких химических катализаторов, главное условие ее получения только соответствующий термический режим. Благодаря этому в процессе изготовления изготавливается полностью натуральный материал, допускается содержание в извести небольших примесей глины.
Известняк имеет формулу CaCO3, так как преимущественно состоит из кальция. В процессе температурного воздействия углекислый газ высвобождается и произведенное сырье имеет формулу CaO.
Процесс контакта кусковой извести с водой выглядит так — CaO + H2O ? Ca(OH)2, существует определенный термин этой реакции, обозначаемый как гашение извести.
Разгашенная известь может находиться в нескольких состояниях:
- Пушонка или мелкий порошок получается в результате смешивания кусков извести с водой, причем процент влаги должен составлять от 60 до 70%.
- Известковое тесто — это соединение исходного материала с водой, ее требуется примерно в 3,5 раза больше. В результате такого гашения образуется плотная масса, используемая в разных сферах.
- Если развести куски извести с водой в соотношении 1:10, то можно получить известковое молоко. Такую гашеную известь используют для побелки внутренних помещений зданий, фасадов, хозяйственных пристроек.
- Если гашеная известь долгое время не используется, то происходит обратный процесс, то есть раствор поглощает углекислый газ и твердеет. В продаже чаще всего можно встретить известь – пушонку или кусковую.
Фото молотой строительной извести

Откуда берутся школьные мелки
Каждый ребенок знает обычный мел, не раз держал его у доски или рисовал на асфальте. А сколько открытий и истин было совершено с помощью ничем не примечательного белого кусочка. Как же из рассыпчатого порошка получаются прочные кирпичики? Может его смешивают с клеем? Оказывается, главное связующее вещество — гипс, а способ изготовления называется метод литья.
Предварительно очищенный от песчинок меловой порошок смешивают в смесителе с гипсом и красителями. Затем смесь ссыпают в бочку и вручную разводят до получения однородной массы. Готовый раствор с помощью шпателя в течение 15 минут, пока он не застыл, разливают по резиновым пресс-формам. Гипс, как и цемент, быстро схватывается, вступая в реакцию с водой.

После того как смесь застынет, изделия извлекают из формы. Для этого ее накрывают металлической решеткой и аккуратно переворачивают, а затем легким постукиванием мелки выбивают из ячеек и отправляют в печь. В течение 40 минут вся содержащаяся в них влага испаряется, и кирпичики мела становятся твердыми и готовыми к использованию.
Человечество всегда будет волновать тема окружающего мира, каким он станет в будущем. По многочисленным докладам и сообщениям ученых, численность населения к 2100 году достигнет 10 миллиардов человек, что неминуемо приведет к истощению минеральных ресурсов, на образование которых потребовались миллионы лет. Главный путь решения проблемы — рациональное и комплексное использование исчерпаемых и невозобновляемых ресурсов.
Технические требования
2.1. Известь следует изготовлять в соответствии с требованиями настоящего стандарта по технологическому регламенту, утвержденному в установленном порядке.
(Измененная редакция, Изм. № 1).
2.2. Материалы, применяемые при производстве извести: карбонатные породы, минеральные добавки (гранулированные доменные или электротермофосфорные шлаки, активные минеральные добавки, кварцевые пески), должны удовлетворять требованиям соответствующих действующих нормативных документов.
2.2.1. Минеральные добавки вводят в порошкообразную известь в количествах, допускаемых требованиями к содержанию в ней активных CaO+MgO по п. 2.4.
2.3. Воздушную негашеную известь без добавок подразделяют на три сорта: 1, 2 и 3; негашеную порошкообразную с добавками — на два сорта: 1 и 2; гидратную (гашеную) без добавок и с добавками — на два сорта: 1 и 2.
2.4. Воздушная известь должна соответствовать требованиям, указанным в табл. 1.
(Измененная редакция, Изм. № 1).
2.4.1. Влажность гидратной извести не должна быть более 5%.
2.4.2. Сортность извести определяют по величине показателя, соответствующего низшему сорту, если по отдельным показателям она соответствует разным сортам.
2.5. (Исключен, Изм. № 1).
Таблица 1
| Норма для извести, %, по массе | ||||||||
| Наименование | негашеной | |||||||
| показателя | кальциевой | магнезиальной и доломитовой | гидратной | |||||
| сорт | ||||||||
| 1 | 2 | 3 | 1 | 2 | 3 | 1 | 2 | |
| Активные
СаО+MgO, не менее: |
||||||||
| — без добавок | 90 | 80 | 70 | 85 | 75 | 65 | 67 | 60 |
| — с добавками | 65 | 55 | — | 60 | 50 | — | 50 | 40 |
| Активный MgO,
не более |
5 | 5 | 5 | 20(40) | 20(40) | 20(40) | — | — |
| СО не более: | ||||||||
| — без добавок | 3 | 5 | 7 | 5 | 8 | 11 | 3 | 5 |
| — с добавками | 4 | 6 | — | 6 | 9 | — | 2 | 4 |
| Непогасившиеся зерна, не более | 7 | 11 | 14 | 10 | 15 | 20 | — | — |
Примечания:
1. В скобках указано содержание MgO для доломитовой извести.
2. СО в извести с добавками определяют газообъемным методом.
3. Для кальциевой извести 3-го сорта, используемой для технологических целей, допускается по согласованию с потребителями содержание непогасившихся зерен не более 20%.
2.6. Гидравлическая известь по химическому составу должна соответствовать требованиям, указанным в табл. 2.
Таблица 2
| Химический | Норма для извести, %, по массе | |
| состав | слабогидравлической | сильногидравлической |
| Активные СаО+MgO: | ||
| — не более | 65 | 40 |
| — не менее | 40 | 5 |
| Активный MgO, не более | 6 | 6 |
| СО, не более | 6 | 5 |
2.7. Предел прочности образцов, МПа (кгс/см), через 28 сут твердения должен быть не менее:
а) при изгибе:
0,4(4,0) — для слабогидравлической извести;
1,0(10) — » сильногидравлической «
б) при сжатии:
1,7(17) — для слабогидравлической извести;
5,0(50) — » сильногидравлической «
2.7.1. Вид гидравлической извести определяют по пределу прочности при сжатии, если по отдельным показателям она относится к разным видам.
2.8. Содержание гидратной воды в негашеной извести не должно быть более 2%.
2.9. Степень дисперсности порошкообразной воздушной и гидравлической извести должна быть такой, чтобы при просеивании пробы извести сквозь сито с сетками № 02 и № 008 по ГОСТ 6613 проходило соответственно не менее 98,5 и 85% массы просеиваемой пробы.
Максимальный размер кусков дробленой извести не должен быть более 20 мм.
(Измененная редакция, Изм. № 1).
2.9.1. По согласованию с потребителем допускается поставка комовой гидравлической извести, используемой в технологических целях.
2.10. Воздушная и гидравлическая известь должна выдерживать испытание на равномерность изменения объема.
Моль
Все вещества состоят из атомов и молекул
В химии важно точно измерять массу веществ, вступающих в реакцию и получающихся в результате нее. По определению моль является единицей количества вещества в СИ
Один моль содержит точно 6,02214076×10²³ элементарных частиц. Это значение численно равно константе Авогадро N A , если выражено в единицах моль⁻¹ и называется числом Авогадро. Количество вещества (символ n
) системы является мерой количества структурных элементов. Структурным элементом может быть атом, молекула, ион, электрон или любая частица или группа частиц.
Постоянная Авогадро N A = 6.02214076×10²³ моль⁻¹. Число Авогадро — 6.02214076×10²³.
Другими словами моль — это количество вещества, равное по массе сумме атомных масс атомов и молекул вещества, умноженное на число Авогадро. Единица количества вещества моль является одной из семи основных единиц системы СИ и обозначается моль. Поскольку название единицы и ее условное обозначение совпадают, следует отметить, что условное обозначение не склоняется, в отличие от названия единицы, которую можно склонять по обычным правилам русского языка. Один моль чистого углерода-12 равен точно 12 г.
Химическая формула и состав вещества (щелочь + вода)
Состав гашеной извести довольно простой и понятный. Данное вещество состоит всего лишь из оксидов кальция, соединенных между собой в определенной последовательности. Получение гидроксида кальция считается также элементарным. Его умели производить в течение многих тысячелетий.
Для этого необходимо всего лишь добавить воду в оксид кальция, после чего данные компоненты нужно хорошо и тщательно между собой перемешать.
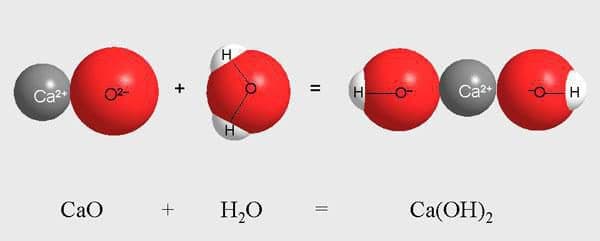
Формула
При заливке оксида кальция водой получается известь, характеристики которой напрямую зависят от времени воздействия друг на друга первоначальных компонентов.
Если перемешивание длилось до 8 минут, то можно говорить о быстрогасящейся извести, около 25 минут – среднегасейщейся, а более получаса – долгогасящейся. Гашеная известь формула Са(ОН)2 – это соединение, водный раствор которого имеет щелочь.
Сфера применения известкового раствора
Гашеная известь благодаря своим свойствам обрела очень широкую сферу применения. Ее используют, как в личных целях многие люди, так и промышленности, как в строительстве различного рода объектов, так дезинфекции. Стоит выделить следующие конкретные способы применения данного вещества:
для побелки деревьев – известь позволяет защитить их от некоторого рода вредителей;

Побелка деревьев
при побелке внутренних помещений сооружений для проведения дезинфекции;

Проведение дезинфекции
для окрашивания деревянных изделий, чтобы продлить им срок эксплуатации, защитив таким образом от процессов гниения и возгорания;

Окрашивание деревянных поверхностей
для изготовления хлорки, применяемой преимущественно для дезинфекции;

Хлорка
в качестве связующего материала в различных строительных растворах. Здесь пропорции цементно известкового раствора для штукатурки;

Соединительный раствор
при изготовлении силикатного бетона. Здесь о расходе цемента на 1 куб бетона;

Силикатный бетон
для изготовления удобрений в землю, повышающих производительность урожая;

Удобрение
- для дубления кож, как один из компонентов технологического процесса;
- для нейтрализации повышенной кислотности в случаях применения в соединениях с Са;
- для изготовления пищевых добавок, прежде всего Е526;
- для обнаружения наличия углекислого газа;
- в изготовлении сахара, используя известковое молоко;
- при необходимости дезинфекции зубов в стоматологических клиниках.
Кроме вышеперечисленных сфер, натронная известь применяется еще со многими другими целями. Тут формула натронной извести. Прежде всего на это повлияли ее очень полезные свойства и технические характеристики.
Подробнее о применении извести смотрите на видео:
Ссылки [ править ]
^ а б Хейнс, Уильям М., изд. (2011). CRC Справочник по химии и физике (92-е изд.). Бока-Ратон, Флорида: CRC Press . п. 4.55. ISBN 1439855110.
^ Calciumoxid Архивировано 30 декабря 2013 г. в Wayback Machine . База данных GESTIS
^ a b Zumdahl, Стивен С. (2009). Химические принципы 6-е изд . Компания Houghton Mifflin. п. A21. ISBN 978-0-618-94690-7.
^ a b c d Карманный справочник NIOSH по химической опасности. «# 0093» . Национальный институт охраны труда и здоровья (NIOSH).
^ «Free Lime «. Архивировано 9 декабря 2017 г. в Wayback Machine . DictionaryOfConstruction.com.
^ Индекс Мерк химических веществ и лекарств, 9-е издание монографии 1650 г.
^ Миллер, М. Майкл (2007). «Лайм». Ежегодник полезных ископаемых . Геологическая служба США . п. 43.13.
^ a b c d e f Тони Оутс (2007), «Известь и известняк», Энциклопедия промышленной химии Ульмана (7-е изд.), Wiley, стр. 1–32, DOI10.1002 / 14356007.a15_317 , ISBN 978-3527306732
^ Колли, Роберт Л. «Солнечная система отопления» Патент США 3,955,554, выданный 11 мая 1976 г.
^ Греттон, Лел. «Сила извести для приготовления пищи — от средневековых горшков до банок 21 века» . Старый и интересный . Проверено 13 февраля 2018 .
^ «Резюме соединения для CID 14778 — оксид кальция» . PubChem.
^ Грей, Теодор (сентябрь 2007 г.). «Limelight in the Limelight» . Популярная наука : 84.
^ Неолитический человек: первый лесоруб? . Phys.org (9 августа 2012 г.). Проверено 22 января 2013.
^ Карканас, P .; Стратули, Г. (2011)
«Неолитические известковые оштукатуренные полы в пещере Дракаина, остров Кефалония, Западная Греция: свидетельство важности этого места». Ежегодник Британской школы в Афинах
103 : 27–41. DOI10.1017 / S006824540000006X .
^ Коннелли, Эшли Николь (май 2012 г.) Анализ и интерпретация неолитических ближневосточных ритуалов погребения с точки зрения сообщества . Диссертация Бейлорского университета, Техас
^ Уокер, Томас A (1888). Тоннель Северн, его строительство и трудности . Лондон: Ричард Бентли и сын. п. 92 .
^ «Научные и производственные заметки». Манчестер Таймс . Манчестер, Англия: 8. 13 мая 1882 года.
^ Патент США 255042, 14 марта 1882
^ Schotsmans, Элин MJ; Дентон, Джон; Декейрсшир, Джессика; Иванеану, Татьяна; Леентес, Сара; Janaway, Роб С .; Уилсон, Эндрю С. (апрель 2012 г.). «Влияние гашеной извести и негашеной извести на разложение захороненных человеческих останков с использованием трупов свиней в качестве аналогов человеческого тела» . Международная криминалистическая экспертиза . 217 (1–3): 50–59. DOI10.1016 / j.forsciint.2011.09.025 . PMID 22030481 .
^ Плутарх , «Серторий 17.1-7» , Параллельные жизни.
↑ Адриенн Майор (2005), «Древняя война и токсикология», в Филиппе Векслере (редактор), Энциклопедия токсикологии , 4 (2-е изд.), Elsevier, стр. 117–121, ISBN 0-12-745354-7
^ Croddy, Эрик (2002). Химическая и биологическая война: всестороннее обследование для заинтересованного гражданина . Springer. п. 128. ISBN 0-387-95076-1.
^ Дэвид Хьюм (1756). История Англии . Я .
Перейти ↑ Sayers, W. (2006). «Использование негашеной извести в средневековой морской войне». Зеркало моряка . Том 92. Выпуск 3. С. 262–269.
^ https://prd-wret.s3-us-west-2.amazonaws.com/assets/palladium/production/atoms/files/mcs-2019-lime.pdf
^ Паспорт безопасности данных CaO, заархивированный 01.05.2012 в Wayback Machine . hazar.com
^ https://www.mindat.org/min-2401.html
^ https://www.ima-mineralogy.org/Minlist.htm
Получение карбоната кальция:
Промышленный способ получения карбоната кальция заключается в разработке его месторождений в природе.
В лаборатории карбонат кальция получают гашением негашеной извести и последующим продуванием углекислого газа.
Оксид кальция (негашеная известь) смешивается с водой. В результате образуется так называемое известковое молоко (гидроксид кальция).
CaO + H2O → Ca(OH)2.
Так как гидроксид кальция растворяется в воде в небольшом количестве, то после отфильтровывания известкового молока получается прозрачный раствор – известковая вода, которая мутнеет при пропускании через неё диоксида углерода (углекислого газа). В результате образуется карбонат кальция, который выпадает в осадок.
Ca(OH)2 + CO2 → CaCO3.
Подготовка [ править ]
Оксид кальция обычно получают в результате термического разложения материалов, таких как известняк или ракушки , которые содержат карбонат кальция (CaCO 3 ; минеральный кальцит ) в печи для обжига извести . Это достигается путем нагревания материала до температуры выше 825 ° C (1517 ° F) в процессе, называемом кальцинированием или обжигом извести , чтобы высвободить молекулу диоксида углерода (CO 2 ) и оставить негашеную известь.
- CaCO 3 (тв) → CaO (тв) + CO 2 (г)
Негашеная известь нестабильна и при охлаждении самопроизвольно реагирует с CO 2 из воздуха до тех пор, пока через достаточное время не превратится обратно в карбонат кальция, если ее не гашить водой до образования известковой штукатурки или известкового раствора .
Ежегодное мировое производство негашеной извести составляет около 283 миллионов тонн. Китай, безусловно, является крупнейшим производителем в мире с общим объемом производства около 170 миллионов тонн в год. Соединенные Штаты — следующие по величине, около 20 миллионов тонн в год.
На 1,0 т негашеной извести требуется примерно 1,8 т известняка . Негашеная известь имеет высокое сродство к воде и является более эффективным осушителем, чем силикагель . Реакция негашеной извести с водой связана с увеличением объема не менее чем в 2,5 раза.
Добыча
Ранее для создания негашеной извести использовали тепловые способы обработки, сегодня данный метод устарел. Причина в выделение диоксида углерода. Альтернативный и предпочтительный метод – это термическое воздействие на кальциевые соли с содержанием кислорода. Приготовление выполняется в несколько этапов.
Устройства для обжига бывают:
кольцевыми;

Печь кольцевая
вращающимися;

Печь вращающаяся
напольными;

Печь напольная
шахтными.

Печь шахтная
Большинство производственных предприятий используют печи шахтного вида, которые работают на газе. Они также бывают пересыпными, когда сырье засыпается сверху и с выносными устройствами для топки.
В сутки печка может произвести порядка 100 т. К недостаткам относится появление в топке золы при прогорании породы, а газовые устройства не требуется чистить.
Самая чистая известь приготовляется в печах, где присутствует выносная топка, тогда не главное, на каком сырье будет работать устройства. Здесь размер печного кирпича. По мощности подобные устройства несколько уступают.
Увеличить качество вещества можно при помощи вращающейся печки, но из-за сложности и дороговизны методики, она практически не применяется. Кольцевые и напольные разновидности печей обладают низкой мощностью и для работы затребуют много топлива, поэтому встречаются только на старых предприятиях.
Что представляет собой гашеная известь?
Известь — это материал, который получается посредством обжига горной породы, относящейся к категории карбонатных. Это может быть, к примеру, известняк или же мел. Известь состоит в основном из оксидов или гидроксидов (в зависимости от конкретного типа материала) таких металлов, как кальций и магний (как правило, наибольший объем занимает оксид или гидроксид кальция). Рассматриваемый материал широко применяется в строительстве.
Если говорить о гашеной разновидности извести, то представлена она в виде щелочного вещества — гидроксида кальция. Данный материал выглядит чаще всего как белый мелкий порошок, слабо растворяющийся в воде. Его температура на ощупь примерно соответствует температуре окружающего воздуха.
Непосредственно гашение извести осуществляется при смешивании негашеной — то есть оксида кальция — с водой. Данная процедура сопровождается ощутимым тепловыделением — порядка 67 кДж на моль.
Гашеная известь — материал, который может применяться:
- как составная часть побелки;
- для защиты деревянных конструкций от разрушения и возгорания;
- в целях приготовления различных строительных растворов;
- для снижения жесткости воды;
- при производстве различных удобрений;
- как пищевая добавка;
- в целях дезинфекции при стоматологических процедурах.
Изучим теперь более подробно специфику основного сырья, используемого для получения гидроксида кальция, то есть негашеной извести.

































