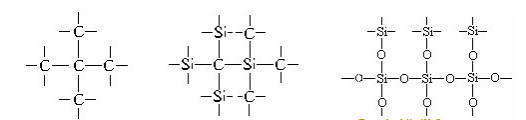
Строение атома. Строение электронных оболочек атомов.
Атом — электронейтральная частица, состоящая из положительно заряженного ядра и отрицательно заряженной электронной оболочки. Ядро находится в центре атома и состоит из положительно заряженных протонов и незаряженных нейтронов, удерживаемых ядерными силами. Ядерное строение атома экспериментально доказал в 1911 г. английский физик Э.Резерфорд.
Число протонов определяет положительный заряд ядра и равно порядковому номеру элемента. Число нейтронов вычисляется как разность атомной массы и порядкового номера элемента. Элементы, имеющие одинаковый заряд ядра (одинаковое число протонов), но разную атомную массу (разное количество нейтронов) называются изотопами. Масса атома в основном сосредоточена в ядре, т.к. ничтожно малой массой электронов можно пренебречь. Атомная масса равна сумме масс всех протонов и всех нейтронов ядра.
Химический элемент — это вид атомов с одинаковым зарядом ядра. В настоящее время известно 118 различных химических элементов.
Все электроны атома образуют его электронную оболочку. Электронная оболочка имеет отрицательный заряд, равный общему количеству электронов. Число электронов в оболочке атома совпадает с числом протонов в ядре и равно порядковому номеру элемента. Электроны в оболочке распределены по электронным слоям согласно запасам энергии (электроны с близкими значениями энергий образуют один электронный слой): электроны с меньшей энергией находятся ближе к ядру, электроны с большей энергией находятся дальше от ядра. Число электронных слоёв (энергетических уровней) совпадает с номером периода, в котором располагается химический элемент.
Различают завершённые и незавершённые энергетические уровни. Уровень считается завершённым, если содержит максимально возможное количество электронов ( первый уровень — 2 электрона, второй уровень — 8 электронов, третий уровень — 18 электронов, четвёртый уровень — 32 электрона и т.д.). Незавершённый уровень содержит меньшее число электронов.
Уровень, максимально удалённый от ядра атома, называется внешним. Электроны, находящиеся на внешнем энергетическом уровне, называются внешними (валентными) электронами. Число электронов на внешнем энергетическом уровне совпадает с номером группы, в которой находится химический элемент. Внешний уровень считается завершённым, если содержит 8 электронов. Завершённым внешним энергетическим уровнем обладают атомы элементов 8А группы (инертные газы гелий, неон, криптон, ксенон, радон).
Область пространства вокруг ядра атома, в которой наиболее вероятно нахождение электрона, называют электронной орбиталью. Орбитали отличаются уровнем энергии и формой. По форме различают s-орбитали (сфера), p-орбитали (объёмная восьмёрка), d-орбитали и f-орбитали. На каждом энергетическом уровне есть свой набор орбиталей: на первом энергетическом уровне — одна s-орбиталь, на втором энергетическом уровне — одна s- и три p-орбитали, на третьем энергетическом уровне — одна s-, три p-, пять d-орбиталей, на четвертом энергетическом уровне одна s-, три p-, пять d-орбиталей и семь f-орбиталей. На каждой орбитале могут располагаться максимально два электрона.
Распределение электронов по орбиталям отражается с помощью электронных формул. Например, для атома магния распределение электронов по энергетическим уровням будет следующим: 2е, 8е, 2е. Данная формула показывает, что 12 электронов атома магния распределены по трём энергетическим уровням: первый уровень завершён и содержит 2 электрона, второй уровень завершён и содержит 8 электронов, третий уровень не завершён, т.к. содержит 2 электрона. Для атома кальция распределение электронов по энергетическим уровням будет следующим: 2е, 8е, 8е, 2е. Данная формула показывает, что 20 электронов кальция распределены по четырём энергетическим уровням: первый уровень завершён и содержит 2 электрона, второй уровень завершён и содержит 8 электронов, третий уровень не завершён, т.к. содержит 8 электронов, четвёртый уровень не завершён, т.к. содержит 2 электрона.
Последнее изменение: Четверг, 12 февраля 2015, 23:41
Опасность здоровью
Кадмий — один из немногих элементов, не выполняет конструктивных функций в человеческом организме. Этот элемент и его соединения являются чрезвычайно токсичными даже в незначительных концентрациях. Имеет свойство накапливаться в организмах и экосистемах.
Вдыхание кадмиевого пыли быстро приводит к заболеваниям, часто смертельных, дыхательных путей и почек (чаще всего — почечная недостаточность). Поглощение любой значительного количества кадмия вызывает немедленное поражение печени и почек. Соединения, содержащие кадмий также канцерогенными. Данные о канцерогенности кадмия ограничены. В опытах на животных не было зафиксировано роста числа опухолей из употребления кадмия. Такая тенденция наблюдалась только с вдыханием частиц пыли, содержащий неорганические соединения кадмия.
Отравление кадмием является причиной болезни, которая впервые была описана в Японии в 50-х годах XX века и получила название «Итай-итай» (что дословно означает «больно-больно»).
Токсичен ли кадмий
Этот химический элемент может попасть в организм с табачным дымом, дорожной пылью. Он находится в дыме теплоэлектростанций, дыме, образующегося после сжигания дров. Любители пива рискуют получить некоторую дозу элемента, потому что его добавляют в напиток для повышения пенообразования.
Японские ученые доказали, что у людей, которые проживают на территориях, загрязненных солями Cd, обнаруживается высокая ломкость костей. Впервые эта болезнь была замечена у фермеров, которые применяли воду с цинковой шахты для орошения рисового поля. Поразительно, но с рисом каждую неделю в организм человека поступало до 4 мг металла (в 8 раз больше предельной нормы).
Вещество угнетает активность ферментов, поражает нервную систему, печень, почки. Хроническая интоксикация приводит к развитию анемии. Пары оксидов и чистого металла токсичны: вдыхание на протяжении полуминуты воздуха с концентрацией паров 5 граммов на кубический метр оказывает смертельное влияние на организм. Острое отравление сопровождается рвотой и судорогами.

Презентация на тему: » Составления электронных и электронно-графических схем строения атома.» — Транскрипт:
1
Составления электронных и электронно-графических схем строения атома

2
Терминологический диктант Электрон Атомная орбиталь Электронная оболочка Энергетический уровень Энергетический подуровень

3
Чтобы правильно изображать электронные конфигурации атомов, нужно ответить на вопросы: 1. Как определить общее число электронов в атоме? 2. Каково максимальное число электронов на уровнях, подуровнях? 3. Какой порядок заполнения подуровней и орбиталей? 3

4
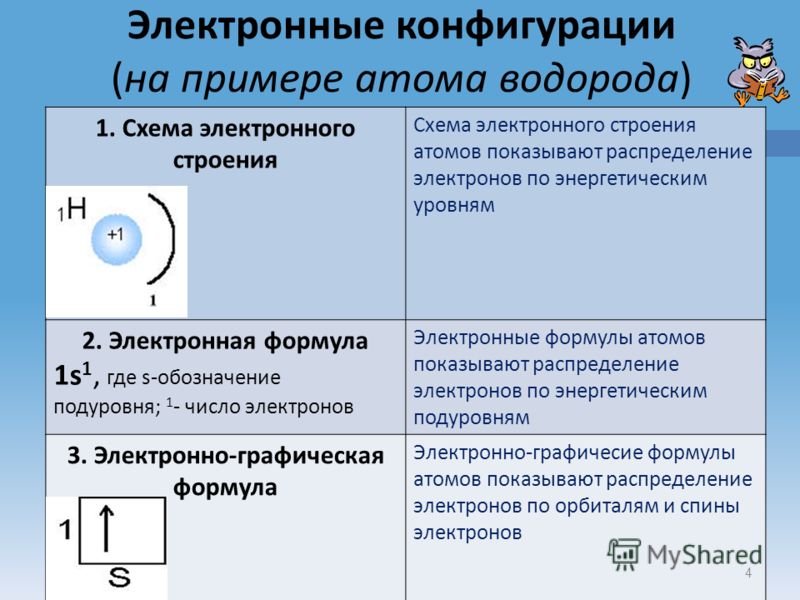
Электронные конфигурации (на примере атома водорода) 1. Схема электронного строения Схема электронного строения атомов показывают распределение электронов по энергетическим уровням 2. Электронная формула 1s 1, где s-обозначение подуровня; 1 — число электронов Электронные формулы атомов показывают распределение электронов по энергетическим подуровням 3. Электронно-графическая формула Электронно-графичесие формулы атомов показывают распределение электронов по орбиталям и спины электронов 4
5
1. Запиши знак химического элемента алюминия. Перед ним внизу укажи его порядковый номер. 5 Al 13

6
2. По образцу составь электронную формулу алюминия Порядок заполнения энергетических уровней в атоме. 1s 2, 2s 2, 2p 6, 3s 2, 3p 1 6 У алюминия 13 электронов Первым в атоме заполняется 1s подуровень На нем максимально может быть 2 электрона, отметим их и вычтем из общего числа электронов. Осталось разместить 11 электронов. Заполняется следующий 2s подуровень, на нем может быть 2 электрона. Осталось разместить 9 электронов. Заполняется следующий 2p подуровень, на нем может быть 6 электронов. Далее заполняем 3s подуровень Дошли до 3p подуровня, на нем максимально может быть 6 электронов, но осталось только 1, его и помещаем. 1s = Al s2s2s 2p2p 3p — 2 = — 6 = — 2 = 9 3 1

7
3. Определи: По порядку ли идут энергетические уровни. Если уровни идут по порядку, то так их и оставь. Если уровни идут не по порядку, то перепиши их, расставив по возрастанию. Нет. 4s и 3d подуровни идут не по порядку. Надо переписать и расставить их по мере возрастания. 7 Cr 24 1s 2 2p62p6 3s 2 4s 2 3p 6 3d 4 2s22s2 1s 2 2p62p6 3s 2 4s 2 3p 6 3d 4 2s22s2

8
Правила для составления электронно-графической схемы Каждый подуровень имеет определенное число орбиталей На каждой орбитали могут находиться не более двух электронов Если на орбитале два электрона, то у них должен быть разный спин (стрелки смотрят в разные стороны). 8 s p d f Приступаем к составлению электронно-графической схемы

9
4. Составь электронно-графическую схемы для хлора 9 Cl 17 1s 2 2p62p6 3s 2 2s22s2 1s 2 2p62p6 3s 2 3p 5 2s22s2 1s 2 2p62p6 3s 2 3p 5 2s22s2

10
5. Географическое путешествие Определите, в каких группах периодической системы находятся химические элементы, электронные формулы атомов которых приведены в первом столбце таблицы. Буквы, соответствующие правильным ответам, дадут название стране. 10 ЯМАЙКА Электронные формулы Группы IIIIIIIVVVIVII 1s 2 2s 1 ЯГЛРКАО 1s 2 2s 2 2p 6 3s 2 3p 5 ВИСНПДМ 1s 2 2s 2 2p 6 3s 2 3p 4 ЕФТЗЯАО 1s 2 2s 2 2p 4 ГРИСЬЙК 1s 2 2s 2 2p 6 3s 2 3p 6 4s 1 КУЕРМИП 1s 2 2s 2 2p 6 3s 1 АНДЛОЖЛ
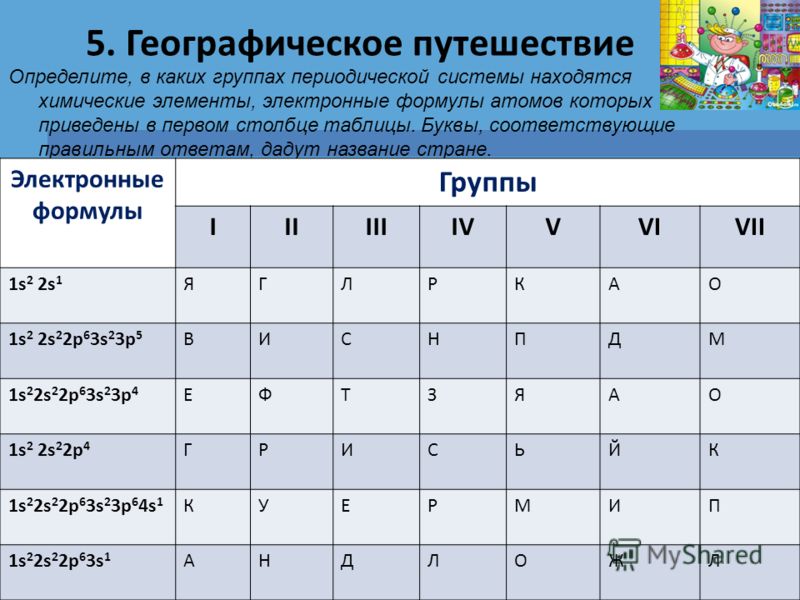
Составляем электронные формулы элементов без всяких расчетов(алгоритмы советской школы).
Здравствуйте, уважаемые читатели!
Обучение школьников составлению электронных формул химических элементов в большинстве случае производится в соответствии со следующим алгоритмом: (https://www.calc.ru/Elektronnaya-Formula-Elementa.html).
2. По номеру периода, в котором расположен элемент, определите число энергетических уровней; число электронов на последнем электронном уровне соответствует номеру группы.
3. Уровни разбить на подуровни и орбитали и заполнить их электронами в соответствии с правилами заполнения орбиталей
Необходимо помнить, что на первом уровне находится максимум 2 электрона 1s2, на втором – максимум 8 (два s и шесть р: 2s22p6), на третьем – максимум 18 ( два s, шесть p, и десять d: 3s2 3p6 3d10).
- Главное квантовое число n должно быть минимально.
- Первым заполняется s-подуровень, затем р-, d- b f-подуровни.
- Электроны заполняют орбитали в порядке возрастания энергии орбиталей (правило Клечковского).
- В пределах подуровня электроны сначала по одному занимают свободные орбитали, и только после этого образуют пары (правило Хунда).
- На одной орбитали не может быть больше двух электронов (принцип Паули).
Как правило, использование этого алгоритма подразумевает распределение электронов по уровням и подуровням с помощью расчетов , т. е на основе постоянного сравнения количества уже учтенных в электронной формуле электронов с общим количеством электронов в атомов. Использование же таблицы Менделеева при этом минимально.
Это можно проследить на множестве обучающих видеоматериалов, в которых авторы обращаются к ТМ практически только за порядковым номером элемента:
или используют ее раскраску:
Проанализировав более 20 видеоматериалов на данную тему, я смогла найти только один, в котором в качестве основы составления формул использовались не расчеты и не искусственные подсказки в виде разной раскраски знаков элементов, а сама структура таблицы Менделеева (10-12 минуты видео):
Преподавание — творческий процесс, каждый преподаватель выбирает те приемы и алгоритмы, которые близки его психологическим характеристикам. Сказывается также и первоначальное знакомство с данным материалом на уроках химии, когда сам преподаватель был школьником.
Ни в коей мере не претендуя на навязывание алгоритмов, по которым работаю, хочу познакомить (или напомнить), как составлять полные и сокращенные электронные формулы с помощью таблицы Менделеева. С данным приемом я познакомилась на уроках моей мамы в далекие советские годы , а затем — на лекциях и семинарах по неорганике в МИТХТ. Об эффективности этого приема может свидетельствовать то, что электронные формулы элементов четырех периодов легко составляли даже те мои одноклассники, которые с трудом могли посчитать молярную массу.
На приведенном ниже видео я попыталась показать, как, используя 2 источника — алгоритм заполнения электронами орбиталей и таблицу Менделеева, можно легко составлять полные и сокращенные электронные формулы любого химического элемента. Заранее прошу прощения за технические и терминологические ляпы (например, «элемент» вместо «атом»), а также за «жаргонные» словечки (вроде «прощелкать по клеткам»). Дело в том, что это видео -мой первый опыт в создании видеоматериалов.
Источник
Таблица электронных формул атомов химических элементов (2 часть):
| 31 | Галлий | Ga | 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p1 |
| 32 | Германий | Ge | 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p2 |
| 33 | Мышьяк | As | 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p3 |
| 34 | Селен | Se | 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p4 |
| 35 | Бром | Br | 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p5 |
| 36 | Криптон | Kr | 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 |
| 37 | Рубидий | Rb | 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 5s1 |
| 38 | Стронций | Sr | 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 5s2 |
| 39 | Иттрий | Y | 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d1 5s2 |
| 40 | Цирконий | Zr | 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d2 5s2 |
| 41 | Ниобий | Nb | 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d4 5s1 |
| 42 | Молибден | Mo | 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d5 5s1 |
| 43 | Технеций | Tc | 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d5 5s2 |
| 44 | Рутений | Ru | 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d7 5s1 |
| 45 | Родий | Rh | 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d8 5s1 |
| 46 | Палладий | Pd | 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 |
| 47 | Серебро | Ag | 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 5s1 |
| 48 | Кадмий | Cd | 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 5s2 |
| 49 | Индий | In | 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 5s2 5p1 |
| 50 | Олово | Sn | 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 5s2 5p2 |
| 51 | Сурьма | Sb | 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 5s2 5p3 |
| 52 | Теллур | Te | 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 5s2 5p4 |
| 53 | Йод | I | 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 5s2 5p5 |
| 54 | Ксенон | Xe | 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 5s2 5p6 |
| 55 | Цезий | Cs | 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 5s2 5p6 6s1 |
| 56 | Барий | Ba | 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 5s2 5p6 6s2 |
| 57 | Лантан | La | 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 5s2 5p6 5d1 6s2 |
| 58 | Церий | Ce | 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 4f1 5s2 5p6 5d1 6s2 |
| 59 | Празеодим | Pr | 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 4f3 5s2 5p6 6s2 |
| 60 | Неодим | Nd | 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 4f4 5s2 5p6 6s2 |
Изотопы
Природный кадмиум состоит из 6 устойчивых изотопов. Было выявлено 27 устойчивых радиоизотопов: Cd-113 с периодом полураспада 7,7 квадриллионов лет, Cd-109 с периодом полураспада 462,6 дней и Cd-115 с периодом полураспада 53,46 часов. Все остальные радиоактивные изотопы имеют период полураспада менее 2,5 часов и большинство из них имеют период полураспада менее 5 минут. Этот элемент имеет 8 метастабильных состояний, самые стойкие из них: Cd-113 (t ½ 14,1 лет), Cd-115 (t ½ 44,6 дней) и Cd-117 (t ½ 3,36 часов).
Изотопы кадмия имеют атомную массу в пределах от 96,935 Дн (Cd-97) к 129,934 Дн (Cd-138). Основной вид распада наиболее распространенного устойчивого изотопа Cd-112 — это захват электрона и его бета-излучения. Продуктом распада к операции является элемент 47 (серебро), а после — элемент 49 (индий).
Электронные формулы элементов первых четырех периодов
Рассмотрим заполнение электронами оболочки элементов первых четырех периодов. У водорода заполняется самый первый энергетический уровень, s-подуровень, на нем расположен 1 электрон:
+1H 1s1 1s
У гелия 1s-орбиталь полностью заполнена:
+2He 1s2 1s
Поскольку первый энергетический уровень вмещает максимально 2 электрона, у лития начинается заполнение второго энергетического уровня, начиная с орбитали с минимальной энергией — 2s. При этом сначала заполняется первый энергетический уровень:
+3Li 1s22s1 1s 2s
У бериллия 2s-подуровень заполнен:
+4Be 1s22s2 1s 2s
Далее, у бора заполняется p-подуровень второго уровня:
+5B 1s22s22p1 1s 2s 2p
У следующего элемента, углерода, очередной электрон, согласно правилу Хунда, заполняет вакантную орбиталь, а не заполняет частично занятую:
+6C 1s22s22p2 1s 2s 2p
Попробуйте составить электронную и электронно-графическую формулы для следующих элементов, а затем можете проверить себя по ответам конце статьи:
5. Азот
6. Кислород
7. Фтор
У неона завершено заполнение второго энергетического уровня:
+10Ne 1s22s22p6 1s 2s 2p
У натрия начинается заполнение третьего энергетического уровня:
+11Na 1s22s22p63s1 1s 2s 2p 3s
От натрия до аргона заполнение 3-го уровня происходит в том же порядке, что и заполнение 2-го энергетического уровня. Предлагаю составить электронные формулы элементов от магния до аргона самостоятельно, проверить по ответам.
8. Магний
9. Алюминий
10. Кремний
11. Фосфор
12. Сера
13. Хлор
14. Аргон
А вот начиная с 19-го элемента, калия, иногда начинается путаница — заполняется не 3d-орбиталь, а 4s. Ранее мы упоминали в этой статье, что заполнение энергетических уровней и подуровней электронами происходит по энергетическому ряду орбиталей, а не по порядку. Рекомендую повторить его еще раз. Таким образом, формула калия:
+19K 1s22s22p63s23p64s11s 2s 2p3s 3p4s
Для записи дальнейших электронных формул в статье будем использовать сокращенную форму:
+19K 4s1 4s
У кальция 4s-подуровень заполнен:
+20Ca 4s2 4s
У элемента 21, скандия, согласно энергетическому ряду орбиталей, начинается заполнение 3d-подуровня:
+21Sc 3d14s2 4s 3d
Дальнейшее заполнение 3d-подуровня происходит согласно квантовым правилам, от титана до ванадия:
+22Ti 3d24s2 4s 3d
+23V 3d34s2 4s 3d
Однако, у следующего элемента порядок заполнения орбиталей нарушается. Электронная конфигурация хрома такая:
+24Cr 3d54s1 4s 3d
В чём же дело? А дело в том, что при «традиционном» порядке заполнения орбиталей (соответственно, неверном в данном случае — 3d44s2) ровно одна ячейка в d-подуровне оставалась бы незаполненной. Оказалось, что такое заполнение энергетически менее выгодно. А более выгодно, когда d-орбиталь заполнена полностью, хотя бы единичными электронами. Этот лишний электрон переходит с 4s-подуровня. И небольшие затраты энергии на перескок электрона с 4s-подуровня с лихвой покрывает энергетический эффект от заполнения всех 3d-орбиталей. Этот эффект так и называется — «провал» или «проскок» электрона. И наблюдается он, когда d-орбиталь недозаполнена на 1 электрон (по одному электрону в ячейке или по два).
У следующих элементов «традиционный» порядок заполнения орбиталей снова возвращается. Конфигурация марганца:
+25Mn 3d54s2
Аналогично у кобальта и никеля. А вот у меди мы снова наблюдаем провал (проскок) электрона — электрон опять проскакивает с 4s-подуровня на 3d-подуровень:
+29Cu 3d104s1
На цинке завершается заполнение 3d-подуровня:
+30Zn 3d104s2
У следующих элементов, от галлия до криптона, происходит заполнение 4p-подуровня по квантовым правилам. Например, электронная формула галлия:
+31Ga 3d104s24p1
Формулы остальных элементов мы приводить не будем, можете составить их самостоятельно.
Некоторые важные понятия:
Внешний энергетический уровень — это энергетический уровень в атоме с максимальным номером, на котором есть электроны.
Например, у меди (3d104s1) внешний энергетический уровень — четвёртый.
Валентные электроны — электроны в атоме, которые могут участвовать в образовании химической связи. Например, у хрома (+24Cr 3d54s1) валентными являются не только электроны внешнего энергетического уровня (4s1), но и неспаренные электроны на 3d-подуровне, т.к. они могут образовывать химические связи.
Свойства Кадмия
 Кадмий относится к переходным металлам. Он мягкий, тягучий и ковкий.
Кадмий относится к переходным металлам. Он мягкий, тягучий и ковкий.
Характеристики:
- Кристаллическая структура решетки гексагональная.
- У элемента рекордная для металлов теплопроводность в области абсолютного нуля.
- Цвет белый, серебристый.
Кадмий тяжелый металл, наряду с осмием, свинцом, молибденом.
Имеет три модификации; отличить их можно некоторым физическим параметрам.
Химические свойства:
- Оксиды и сульфиды кадмия почти не растворяются в воде.
- В условиях влажного воздуха на поверхности образуется оксидная пленка. Она препятствует дальнейшему окислению.
- Не образует карбидов.
- В нагретых разбавленных H2SO4 и HNO3 (формулы серной и соляной кислот) кадмий растворяется с выделением водорода.
| Ка́дмий / Cadmium (Cd), 48 |
| 112,411(8) а. е. м. (г/моль) |
| 4d10 5s2 |
| 154 пм |
| 148 пм |
| (+2e) 97 пм |
| 1,69 (шкала Полинга) |
| −0,403 |
| 2 |
| 867,2 (8,99) кДж/моль (эВ) |
| 8,65 г/см³ |
| 594,1 K (321 °C) |
| 1038 K (764,85 °C) |
| 6,11 кДж/моль |
| 59,1 кДж/моль |
| 26,0 Дж/(K·моль) |
| 13,1 см³/моль |
| гексагональная |
| a=2,979 c=5,618 Å |
| 1,886 |
| 209 K |
| (300 K) 96,9 Вт/(м·К) |
| 7440-43-9 |
Рекомендуем: РТУТЬ — «кровь дракона» в лампах и реакторах
Физические свойства
Кадмий — это мягкий, тягучий, гибкий, серебристо-белый двухвалентный металл, который можно легко разрезать. Во многом он похож на цинк, но он способен образовывать сложные соединения.
Химические свойства
По химическим свойствам кадмий подобный цинка, однако менее активным. При обычной температуре на воздухе поверхность металлического кадмия покрывается оксидной пленкой, которая затрудняет проведение реакций — большинство взаимодействий проходят при нагревании. При сжигании кадмия в струе кислорода образуется его оксид:
При контакте с водой кадмий пассивируется за появления гидроксидних пленки Cd (OH) 2, однако он активно разлагает перегретый водную пару:
Кроме кислорода, металлический кадмий взаимодействует также с галогенами, серой, селеном, фосфором (с образованием примесей):
Восстановительные свойства в кадмия слабее, чем в цинке, но он так же восстанавливает некоторые неметаллы из оксидов и металлы в их солях (в растворах):
Кадмий может выступать в качестве комплексообразователя, координируя 3, 4 или 6 лигандов:
Электронная схема кадмия
You need to enable JavaScript to run this app.
Одинаковую электронную конфигурацию имеют атом кадмия и +1In, +2Sn, +3Sb, +4Te, +5I, +6Xe
Порядок заполнения оболочек атома кадмия (Cd) электронами: 1s → 2s → 2p → 3s → 3p → 4s → 3d → 4p → 5s → 4d → 5p → 6s → 4f → 5d → 6p → 7s → 5f → 6d → 7p.
На подуровне ‘s’ может находиться до 2 электронов, на ‘s’ — до 6, на ‘d’ — до 10 и на ‘f’ до 14
Кадмий имеет 48 электронов, заполним электронные оболочки в описанном выше порядке:
2 электрона на 1s-подуровне
2 электрона на 2s-подуровне
6 электронов на 2p-подуровне
2 электрона на 3s-подуровне
6 электронов на 3p-подуровне
2 электрона на 4s-подуровне
10 электронов на 3d-подуровне
6 электронов на 4p-подуровне
2 электрона на 5s-подуровне
10 электронов на 4d-подуровне
Степень окисления кадмия
Атомы кадмия в соединениях имеют степени окисления 2, 1.
Степень окисления — это условный заряд атома в соединении: связь в молекуле между атомами основана на разделении электронов, таким образом, если у атома виртуально увеличивается заряд, то степень окисления отрицательная (электроны несут отрицательный заряд), если заряд уменьшается, то степень окисления положительная.
2+Cd 1+Cd
Cd 0
Валентность Cd
Атомы кадмия в соединениях проявляют валентность II, I.
Валентность кадмия характеризует способность атома Cd к образованию хмических связей. Валентность следует из строения электронной оболочки атома, электроны, участвующие в образовании химических соединений называются валентными электронами. Более обширное определение валентности это:
Валентность не имеет знака.
Квантовые числа Cd
Квантовые числа определяются последним электроном в конфигурации, для атома Cd эти числа имеют значение N = 4, L = 2, Ml = -2, Ms = ½
Видео заполнения электронной конфигурации (gif):
Результат:
- Металл соединяют с цирконием, цинком для получения сплавов с улучшенными характеристиками.
- Для увеличение механических свойств сплав дополняется редкоземельными металлами, которые выступают в роли легированных добавок.
- Твердость по системе Бринелля — 20 НВ.